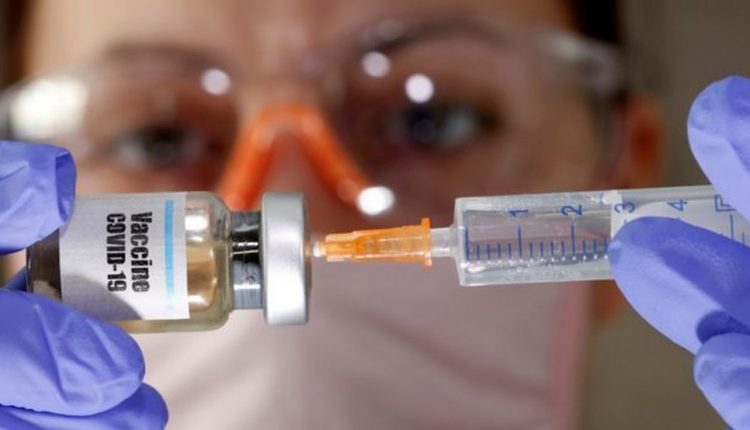
Anvisa autoriza uso emergencial de vacinas contra Covid-19
Agência ainda não recebeu nenhum pedido de registro no país
Apesar de não ter recebido nenhum pedido de uso emergencial e nem pedido de registro de vacinas para Covid-19 no país, a Agência Nacional de Vigilância Sanitária (Anvisa) decidiu nesta quinta-feira (10) que concederá autorização temporária de uso emergencial, em caráter experimental, de vacinas e estabeleceu regras para que empresas solicitem a autorização.
A medida abre caminho para que empresas façam o pedido de emergência. “A autorização de uso emergencial é um mecanismo que pode facilitar a disponibilização e o uso das vacinas contra Covid-19, ainda que não tenham sido avaliadas sob o crivo do registro, desde que cumpram com os requisitos mínimos de segurança, qualidade e eficácia”, disse Alessandra Bastos Soares, diretora da Anvisa.
“Qualquer autorização concedida pela Anvisa, qualquer anuência, só será feita diante de um pleito. A vacina só terá autorização de uso emergencial e experimental se houver o pleito realizado por alguma empresa”, disse Soares que ressalta ainda que poderá modificar, suspender ou cancelar a autorização temporária a qualquer momento, com base em elementos técnicos e científicos.
Quatro vacinas estão em testes de fase 3 no Brasil: a da Pfizer, a de Oxford, a da Johnson e a da Sinovac.
‘Lei Covid’
A aplicação de uma vacina contra a Covid-19 no Brasil depende da aprovação para o uso do novo medicamento. A permissão pode ser conseguida basicamente por dois caminhos: o primeiro está diretamente ligado aos dois tipos de registro (tradicional ou emergencial) que podem ser dados pela Agência Nacional de Vigilância Sanitária (Anvisa) e a segunda possibilidade é baseada na chamada “Lei Covid”, que libera o uso se o imunizante tiver aval expedido por uma agência do exterior, independentemente de registro pela Anvisa.
Anvisa – registro definitivo: os desenvolvedores submetem o pedido de registro à Anvisa apenas após concluírem as 3 fases de testes da vacina. Para acelerar o trâmite, a agência criou o procedimento de submissão contínua de dados.
Anvisa – uso emergencial: permite aos desenvolvedores enviarem os dados que comprovem eficácia e segurança antes de terminarem a fase 3 da vacina;
Lei Covid – Prevê que a Anvisa terá o prazo de 72 horas para conceder a autorização caso o imunizante tenha conseguido registro no Japão, nos EUA, na Europa ou na China. Caso o prazo não seja cumprido e a Anvisa não se manifeste, a autorização é concedida automaticamente.